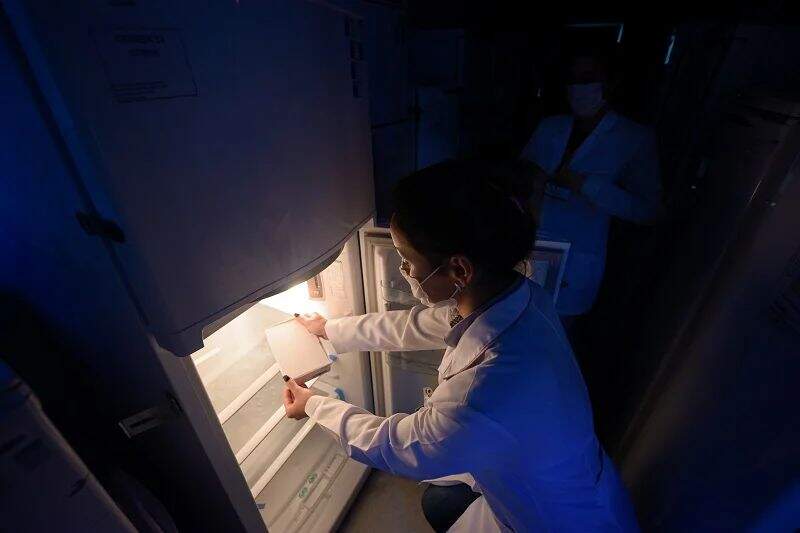
A vacina chinesa que será testada no Brasil já está no HSL-PUCRS (Hospital São Lucas da PUCRS). A equipe da instituição responsável pelo estudo, que já recebeu mais de 5 mil inscrições de interessados, teve acesso ao primeiro lote da Coronavac por volta das 14h desta segunda-feira (3).
A lista com os primeiros profissionais da saúde que serão envolvidos no processo deve ser consolidada nos próximos dias, para que os testes possam ser iniciados na próxima semana. Todas as pessoas confirmadas para participar do procedimento receberão contato do Hospital para agendamento, checagem dos critérios e orientações gerais.
Os 850 profissionais da saúde selecionados serão divididos em grupos e após receberem as injeções, serão monitorados continuamente para a documentação dos resultados. Cada um deverá receber duas doses da vacina ou do placebo, em um intervalo de cerca de duas semanas. A vacinação deverá se estender até o mês de outubro.
Saiba mais
A CoronaVac, vacina contra o novo coronavírus desenvolvida pela farmacêutica chinesa Sinovac Biotech, é uma das mais promissoras em todo o mundo. O Hospital São Lucas, da PUCRS (Pontifícia Universidade Católica do RS), é um dos 12 centros que serão responsáveis pelos testes de fase 3, em humanos.
A vacina utiliza tecnologia já conhecida e amplamente aplicada em outras vacinas. Por isso, o Instituto Butantan avalia que sua incorporação ao sistema de saúde deva ocorrer mais facilmente. Na ocasião do anúncio dos testes, a informação é de que o laboratório com sede em Pequim já havia realizado testes do produto em cerca de mil voluntários na China, nas fases 1 e 2. Antes, o modelo experimental aplicado em macacos apresentou resultados expressivos em termos de resposta imune contra as proteínas do vírus.
Os testes serão realizados em nove mil voluntários em centros de pesquisas de seis Estados brasileiros: São Paulo, Brasília, Rio de Janeiro, Minas Gerais, Rio Grande do Sul e Paraná. A pesquisa clínica será coordenada pelo Instituto Butantan,um dos maiores centros de pesquisa, desenvolvimento e produção de imunobiológicos do mundo.
Na cidade de São Paulo, os testes serão conduzidos pelo Hospital das Clínicas da Faculdade de Medicina da USP, Instituto de Infectologia Emílio Ribas e Hospital Israelita Albert Einstein. Também serão envolvidos no Estado de São Paulo a Universidade Municipal de São Caetano do Sul, Hospital das Clínicas da Unicamp em Campinas, Faculdade de Medicina de São José do Rio Preto e o Centro de Saúde Escola da Faculdade de Medicina da USP de Ribeirão Preto.
As pesquisas estão previstas para realização, ainda, na UnB (Universidade de Brasília), Instituto Nacional de Infectologia Evandro Chagas, no Rio de Janeiro, Centro de Pesquisa e Desenvolvimento de Fármacos da Universidade Federal de Minas Gerais, Hospital São Lucas da PUC do Rio Grande do Sul e Hospital das Clínicas da Universidade Federal do Paraná.
A farmacêutica fornece ao Butantan as doses da vacina para a realização de testes clínicos de fase 3 em voluntários no Brasil, com o objetivo de demonstrar sua eficácia e segurança.
Caso a vacina seja aprovada, a Sinovac e o Butantan vão firmar acordo de transferência de tecnologia para produção em escala industrial tanto na China como no Brasil para fornecimento gratuito ao SUS (Sistema Único de Saúde). Os passos seguintes serão o registro do produto pela Anvisa e fornecimento da vacina em todo o Brasil.